Microbiota intestinale: una definizione (vedi anche Il Microbiota intestinale: un coinquilino indispensabile)
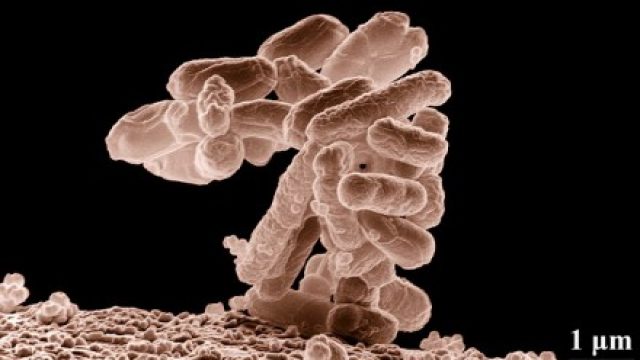
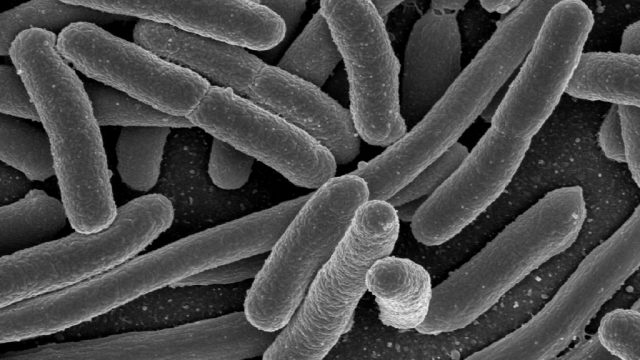
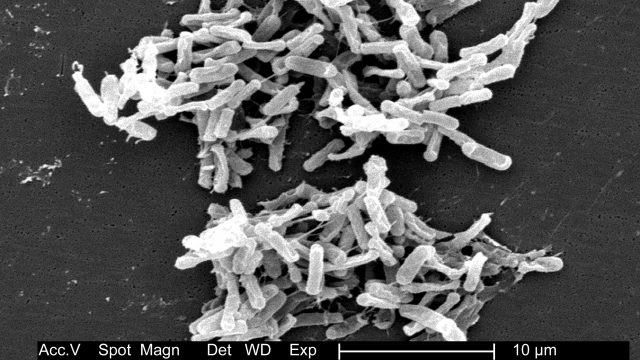
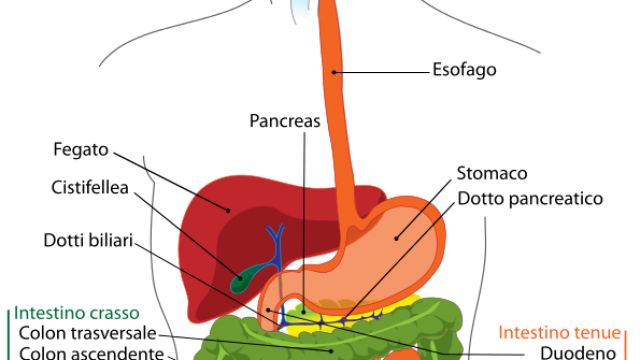
Il corpo umano è abitato da un vasto numero di batteri, archaea, virus ed eucarioti unicellulari, in uno stato di pacifica coesistenza. Questo insieme di microorganismi viene chiamato microbiota. Le cellule del microbiota sono di gran lunga più numerose di quelle umane (le superano di una decina di volte) e colonizzano tutte le superfici del corpo umano che sono a contatto con l’esterno: la pelle, il tratto genito-urinario, quello gastrointestinale e quello respiratorio. La superficie dell’intestino è decisamente ampia (circa 200 mq), e pertanto il tratto intestinale è la porzione del corpo più abbondantemente colonizzata dal microbiota.
Sebbene le specie presenti nell’intestino siano molto numerose (si è arrivati a parlare di 35.000 specie batteriche), sono due le categorie che dominano la flora intestinale: i Bacteroidetes e i Firmicutes. Probacteria, Verrucomicrobia, Actinobacteria, Fusobacteria e Cyanobacteria sono presenti in proporzioni minori.
L’obesità: un fenomeno tanto diffuso e ancora non del tutto compreso
L’obesità è una patologia complessa non ancora completamente compresa, definita dalla WHO (World Health Organization) come un’epidemia globale per la sua massiva diffusione. Le ragioni che spiegano questo fenomeno sono numerose e non si limitano solamente alla ridotta attività fisica associata all’aumentato consumo di pietanze altamente caloriche – contenenti grandi quantità di zuccheri e grassi saturi- e povere di nutrienti. Molti altri fattori possono influenzare questa condizione, tra cui:
- fattori genetici
- patologie sottostanti
- farmaci
- diete ad alto indice glicemico
- stress
- cessazione del fumo
- infezioni virali
- batteri
I batteri che vanno a costituire il microbiota intestinale svolgono un’ampia gamma di attività, tra cui quella di destrutturare alcuni substrati, come le fibre vegetali, che non possono venire completamente idrolizzate dagli enzimi del piccolo intestino. Modulano anche l’assorbimento e la deposizione dei grassi presenti nella dieta. I principali prodotti dovuti alla fermentazione delle fibre di scarto sono gli acidi grassi a catena corta (SCFA, short chain fatty acids), ovvero acetato, propionato e butirrato, che possono essere utilizzati per la sintesi de novo di lipidi o glucosio. Gli acidi grassi a catena corta possono provvedere al 10% dell’energia totale assunta con la dieta e al 60-70% dell’energia che serve all’epitelio del colon per lo svolgimento delle sue normali funzioni. Il propionato è largamente utilizzato dal fegato per la gluconeogenesi, la liponeogenesi e la sintesi proteica, mentre l’acetato è un substrato per la sintesi del colesterolo. Possono anche favorire l’uptake di glucosio intestinale (attraverso l’aumentata espressione del cotrasportatore Na+/glucosio), nonché rendere più efficiente l’idrolisi degli acidi grassi attraverso lo stimolo alla produzione di colipasi. Nel momento in cui si trovino alte concentrazioni di questi acidi grassi nelle feci è possibile pensare a più cause: una maggior produzione da parte del microbiota, un cambiamento dello schema nutrizionale, un ridotto assorbimento intestinale, un maggior transito intestinale o una modificazione dei gruppi batterici che costituiscono il microbiota. Non tutti gli studi presentano risultati univoci su quest’ultimo punto: in alcuni casi l’aumento degli acidi grassi a catena corta è stato ricondotto ad un’alterazione del rapporto fra Firmicutes (batteri gram-negativi) e altre specie batteriche a favore dei primi; in altri è stato osservato un aumento dei Bacteroides spp, la specie più rappresentativa dei Batteroidi. Ulteriori ricerche vanno svolte in questa direzione, ciononostante è facilmente intuibile come l’alimentazione possa avere un peso rilevante nell’influenzare le diverse specie batteriche e come a sua volta queste ultime, favorendo la produzione di acidi grassi a catena corta, facilitino l’accumulo di grassi e l’aumento di peso.
Il microbiota e il sovrappeso
Il microbiota intestinale rende possibile l’idrolisi di polisaccaridi [zuccheri], altrimenti indigeribili, rendendoli monosaccaridi assorbibili. Inoltre attiva la lipoproteina lipasi [enzima che idrolizza i trigliceridi liberando acidi grassi che entrano poi nelle cellule] del tessuto adiposo: la conseguenza è l’eccessivo assorbimento di carboidrati e l’eccessivo accumulo di acidi grassi, con l’aumento di peso che ne deriva.
Un interessante studio sembra dimostrare come un’alterazione della flora intestinale preceda lo sviluppo di sovrappeso. Il ruolo cruciale sarebbe quello rivestito dal Bifidobacterium, che caratterizza il microbiota del primo anno di vita. Tanto più è presente e numeroso a livello dell’intestino dei bimbi piccoli, tanto meno si tenderà a sviluppare sovrappeso. Non solo: una ridotta presenza di S. Aureus nelle feci dei bambini è un fattore favorevole per il mantenimento di un peso nella norma. Si può pertanto concludere che un alto numero di Bifidobatteri e un basso numero di S. Aureus possono offrire una certa protezione contro il sovrappeso e l’obesità.
Allattamento al seno e microbiota intestinale
Anche l’allattamento al seno sembra essere un fattore protettivo: è stato osservato che nei bambini in salute allattati al seno vi è un microbiota caratterizzato da Bifidobacteria (soprattutto B. breve, B. infantis, B. longum). Il latte materno stesso contiene questo tipo di batteri ed anche numerosi polisaccaridi [zuccheri] che favoriscono il sostentamento di queste stesse specie. I bifidobatteri arrivano a costituire il 60-90% della flora intestinale dei neonati, influenzando l’attività metabolica totale del microbiota intestinale, ed il latte materno potrebbe essere un fattore chiave nella regolazione del sistema immunitario e nello sviluppo di tolleranza verso queste popolazioni batteriche.
I bambini, dunque, hanno un microbiota intestinale che viene già parzialmente forgiato al momento del parto, per influsso del microbiota vaginale ed intestinale della madre (vedi anche Il Microbiota intestinale: un coinquilino indispensabile). Il latte materno rafforza questa popolazione. Ulteriori studi stanno valutando l’influenza dei batteri di derivazione cutanea, come lo S. Aureus: è stato osservato come una precoce colonizzazione intestinale da parte di questo batterio sia correlata ad un aumento di un marcatore di infiammazione sistemica (CD14). Giacché a sua volta l’infiammazione è un fattore in grado di favorire l’obesità, lo S. Aureus potrebbe svolgere un ruolo significativo all’interno di questo circolo vizioso.
Conclusioni
Un microbiota in equilibrio è importante per lo svolgimento di molte funzioni, come la protezione da agenti patogeni, la modulazione del sistema immunitario, la regolazione delle capacità di assorbimento dell’epitelio intestinale ed anche il mantenimento di un peso corretto. Sebbene i fattori in grado di influenzare l’equilibrio intestinale siano numerosi, un’alimentazione salutare e varia può favorire una flora batterica sana e migliorare la salute generale.
Vedi anche:
Il Microbiota umano: un coinquilino indispensabile
Il microbiota, l’abuso di antibiotici e l’aumento di peso
Il tessuto adiposo e il microbiota: due organi endocrini in stretta comunicazione
L’intestino: il nostro secondo cervello sensibile alle emozioni
Bibliografia:
- Zhang Y , Li S , Gan R, Zhou T, Xu D and Li H (2015) Impacts of Gut Bacteria on Human Health and Diseases Int. J. Mol. Sci 16: 7493-7519
- Kalliomaki M, Collado MC, Salminen S, and Isolauri (2008) Early differences in fecal microbiota composition in children may predict overweight Am J Clin Nutr 87:534–8
- Schwiertz A,Taras D, Schäfer K, Beijer S, Bos NA, Donus C and Hardt PD (2009) Microbiota and SCFA in Lean and Overweight Healthy Subjects Obesity 18 (1): 190–195
- Duncan SH , Lobley GE, Holtrop G, Ince J, Johnstone AM, Louis P and Flint HJ (2008) Human colonic microbiota associated with diet, obesity and weight loss International Journal of Obesity 32: 1720–1724
- Sekirov I, Russell SL, Caetano L, Antunes M and Brett Finlay B (2010) Gut Microbiota in Health and Disease Physiol Rev 90: 859–904